肿瘤标志物是1978年Herberman在美国国立癌症研究院召开的人类免疫及肿瘤免疫诊断会上提出的,1979年在英国第七届肿瘤发生生物学和医学会议上作为专用术语被大家公认。三十余年来,肿瘤标志物的研究逐渐形成了一门独立的学科分支。
肿瘤标志物,是指在肿瘤发生和增殖过程中,由肿瘤细胞生物合成、释放或是机体对肿瘤细胞反应而产生的一类物质,这些物质可存在于肿瘤细胞和组织中,也可进入血液和其他体液。当肿瘤发生发展时,这些物质明显异常,可以利用生物化学、免疫和分子生物学等技术对其进行定性或定量检测。
肿瘤标志物的血清水平一般与恶性肿瘤的发生、发展、消退、复发等具有良好的相关性,因此测定血清肿瘤标志物水平,可以获得有关恶性肿瘤的诊断、疗效及预后等方面的信息。
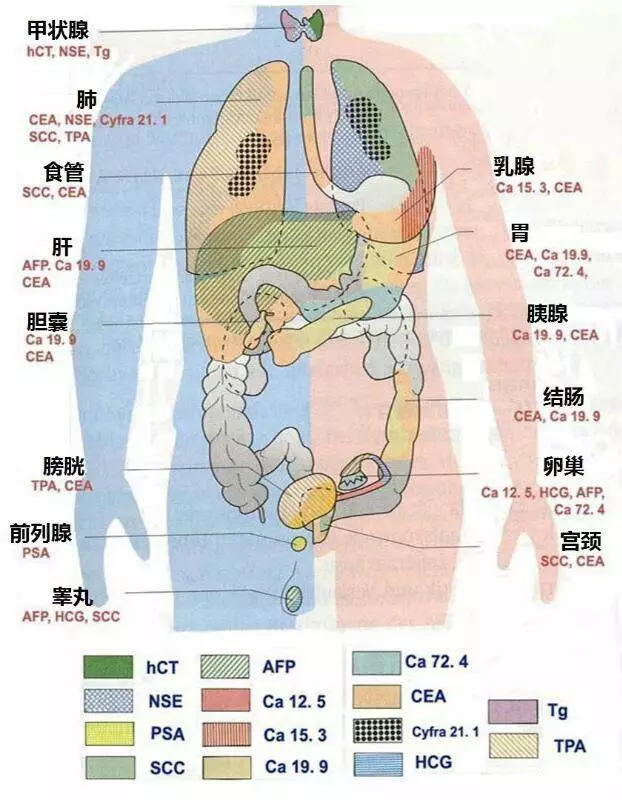
一、高危人群的筛查
早期发现、早期诊断、早期治疗是肿瘤诊治的重要原则。一般认为,利用现代生物物理技术如超声显像、计算机X线断层摄影、磁共振成像等可发现直径1~1.5cm的肿瘤,而肿瘤生长到2~3mm是即可用免疫学诊断方法测出。肿瘤标志物检测是发现无症状患者的重要线索,可作为肿瘤的辅助诊断工具。在所有标志物中,目前能用于普查的只有AFP和PSA,如对慢性乙肝病毒携带者、慢性乙型肝炎和丙型肝炎患者进行AFP检测,可早期发现肝癌;PSA结合直肠指诊亦在世界各地被广泛应用于早期前列腺癌的筛查。
二、肿瘤的鉴别诊断和临床分期
在临床已获得足够证据证明患者可能患某脏器肿瘤后,肿瘤标志物往往能提供有用的信息帮助区分良、恶性肿瘤和肿瘤类型,如CEA和NSE可辅助区分胃肠道肿瘤是腺癌(CEA阳性、NSE阴性)还是类癌(CEA阴性、NSE阳性);血清肿瘤标志物升高的水平与肿瘤的大小和分化程度有关,其定量检测有助于辅助诊断临床分期。
三、肿瘤的复发监测和预后判断
肿瘤标志物的动态监测有助于判断肿瘤是否复发。一般建议,治疗后第6周进行第一次测定,前3年内每3个月测定1次,3~5年每半年测定一次,5~7年每年一次。如发现肿瘤标志物升高(高于首次值25%),应在2~4周后,再测定1次,连续2次升高者,提示复发或转移。
肿瘤标志物浓度增加或降低与肿瘤预后密切相关。Newlands等报道HCG和AFP可作为睾丸癌的预后指标,HCG<50U/L的4年生存率为96%,HCG>50U/L或AFP>500U/L的4年生存率为56%。此外,结肠癌时CEA浓度、非霍奇金淋巴瘤时β2微球蛋白浓度、卵巢癌时CA125浓度等的变化都有预后价值。
四、肿瘤的疗效检测
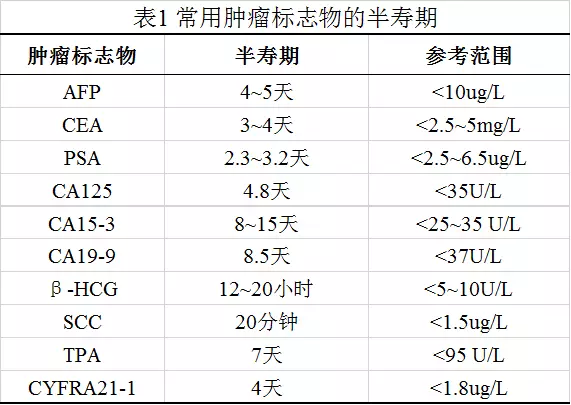
肿瘤标志物有助于明确手术、放疗或药物治疗是否有效。通常在成功的治疗如肿瘤完全切除和有效化疗后,肿瘤标志物即明显下降,若下降至正常或治疗前水平的95%即认为治疗成功;如果术后肿瘤标志物未如预期下降,说明手术未能成功切除肿瘤。肿瘤标志物下降的时间取决于肿瘤标志物的半寿期,表1是常用肿瘤标志物的半寿期。
五、肿瘤标志物的联合检测
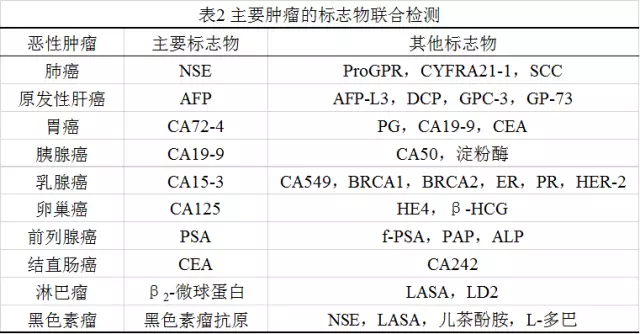
一种肿瘤可产生多种肿瘤标志物,不同的肿瘤或同种肿瘤的不同组织类型可有相同的肿瘤标志物,不同的肿瘤患者体内肿瘤标志物的质和量变化也较大。由于大部分单个肿瘤标志物敏感性或特异性偏低,不能满足临床需要,近10年来,理论和实践上都提倡同时测定多个肿瘤标志物,以提高敏感性和特异性,但联合检测的指标必须经科学分析、严格筛选,在此前提下,合理选择3~5项敏感性高、特异性强的肿瘤标志物进行联合检测,可避免医疗资源的浪费,减轻患者的经济负担。常用肿瘤标志物的组合见表2。
六、肿瘤的个体化医疗
所谓“个体化医疗”,是指在适当的治疗时间,使用适当的给药途径,对适当的患者施以适当的药物和适当剂量,以避免不当治疗和有害治疗,降低药物的毒副作用。识别患者个体差异的依据主要是某些特定的分子标志物(靶标),实现多这些靶标的准确检测和评估是肿瘤个体化医疗的基础。随着新靶向药物的发现及研究的深入,个体化医疗的靶标检测也将从单一靶标检测发展为多靶标联合检测,最终形成靶标检测系统,有望提高靶向治疗的针对性和有效性。
参考文献
1. 李勋, 王昌富. 血清肿瘤标志物检测临床应用需注意的问题[J]. 基层医学论坛, 2013, (25):3349-3350.
2. 陈国栋, 贺更生. 血清肿瘤标志物研发及临床应用评价新进展[J]. 医学综述, 2013, 19(4):632-634.
3. 胡林, 王建新. 血清及腹腔积液肿瘤标志物联合检测的临床应用价值[J]. 现代医药卫生, 2014, (12):1772-1773.
4. Sturgeon CM,Lai LC,Dufly MJ.Serum tumour markers:how to order and interpret them.BMJ,2009,339:b3527.
(内容来源于医学界肿瘤频道,作者:youlin,转载出于传递更多信息之目的,版权和荣誉归原作者所有。如有侵权请联系我们妥善处理!)


